磷脂酶C的克隆表达及酶学性质研究

磷脂酶C的克隆表达及酶学性质研究(任务书,论文10200字)
摘要
本课题通过查阅磷脂酶C相关文献资料,利用序列比对方法获得一条具有磷脂酰胆碱和磷脂酰乙醇胺特异性磷脂酶C活性的基因,通过基因工程手段将其构建至表达载体PMA5上,然后转化至表达宿主枯草芽孢杆菌WB800中进行胞外表达,获得重组菌B.sublitis/PMA5-PCPLC。并且对其发酵所得重组蛋白进行酶学性质研究,结果表明:PC-PLC粗酶液蛋白浓度为0.5 mg/ml,酶活为26.5 U/mg,该酶的最适反应温度为45 ℃,这里面Mg2+和Zn2+对PC-PLC活性有较大的促进作用,而当Co2+存在时,酶活性则受到抑制。
关键字:磷脂酶C 克隆表达 酶学性质
Cloning Expression and Enzymatic Properties of Phospholipase C
ABSTRACT
As a new technology in oil refining, enzyme degumming has several advantages over traditional oil degumming, such as mild reaction condition, wide range of application, less pollution to environment and so on. However, PLC has drew wide attention of oil company not only for its short reaction time, but the efficiency of converting phospholipid into 1,2-Diacylglycerol(1, 2-DAG), which could increase the oil yield obviousely.
In this work, we reviewed the related literature of phospholipase C and obtained a gene with phosphatidylcholine and phosphatidylethanolamine-specific phospholipase C activity using the sequence comparison method. It was constructed by gene engineering into the expression vector PMA5 and then transformed into the expression host Bacillus subtilis WB800 for extracellular expression to obtain the recombinant B.sublitis/PMA5-PCPLC. The enzymatic properties of the recombinant protein obtained from its fermentation were studied. The results showed that the protein concentration of PC-PLC crude enzyme solution was 0.5 mg/ml and the enzyme activity was 26.5 U/mg. The optimum reaction temperature of this enzyme was 45°C. With a suitable pH of 6.0, the enzyme activity is affected by multiple metal ions, of which Mg2+ and Zn2+ have a greater promoting effect on PC-PLC activity, and when Co2+ is present, the enzyme activity is inhibited.
Key Words: Phospholipase C, Cloning Expression, Enzymatic Properties
[资料来源:http://Doc163.com]
[资料来源:https://www.doc163.com]

目 录
摘要…………………………………………………………………………………I
ABSTRACT………………………………………………………………………II
第一章 引言 3
1.1 磷脂酶概述 3
1.2 磷脂酶C的种类及来源 4
1.3 磷脂酶C的研究现状及应用 5
1.4 酶法脱胶 6
1.5 酶法脱胶中酶的比对与选择 7
1.6 本课题研究意义 8
第二章 实验方法 8
2.1 实验材料 8
2.2 实验试剂 9
2.3 培养基及培养方法 10
2.3.1 培养基 10
2.3.2 菌株培养方法 11
第三章 实验内容 11
3.1 蜡状芽孢杆菌基因组提取 11
3.2 目的基因片段的扩增 11
3.3 重组菌E.COLI/PMA5-PCPLC的构建及鉴定 12
3.3.1 质粒PMA5及目的基因PCPLC双酶切 12
3.3.2 重组质粒PMA5-PCPLC构建 12
3.3.3 重组质粒转化至大肠杆菌E. coli DH5α 12
3.3.4 重组质粒鉴定 13
3.4 重组菌B.SUBLITIS/PMA5-PCPLC的构建 13
3.4.1 重组质粒转化至枯草芽孢杆菌 13
3.4.2 重组菌B.sublitis/PMA5-PCPLC的验证 14
3.5 重组蛋白PC-PLC的表达及粗酶液制备 14
3.5.1 重组蛋白PC-PLC的表达 14
3.5.2 硫酸铵分级沉淀制备粗酶液 14
3.6 PC-PLC粗酶液蛋白浓度及酶活测定 14
3.6.1 PC-PLC粗酶液蛋白浓度测定 14
3.6.2 PC-PLC粗酶液酶活测定 15
3.7 PC-PLC粗酶液酶学性质研究 15
3.7.1 重组PC-PLC底物特异性分析 15
3.7.2 最适温度及温度稳定性研究 15
3.7.3 最适pH及pH稳定性研究 15
3.7.4 金属离子影响 16
第四章 结果与讨论 16
4.1 蜡状芽孢杆菌基因组提取 16
4.2 目的基因PC-PLC的PCR扩增 16
4.3 重组质粒的构建及PCR验证 17 [资料来源:www.doc163.com]
4.4 重组PC-PLC蛋白的表达鉴定及粗酶液制备 18
4.5 PC-PLC粗酶液蛋白浓度及酶活测定 20
4.6 PC-PLC底物特异性分析 20
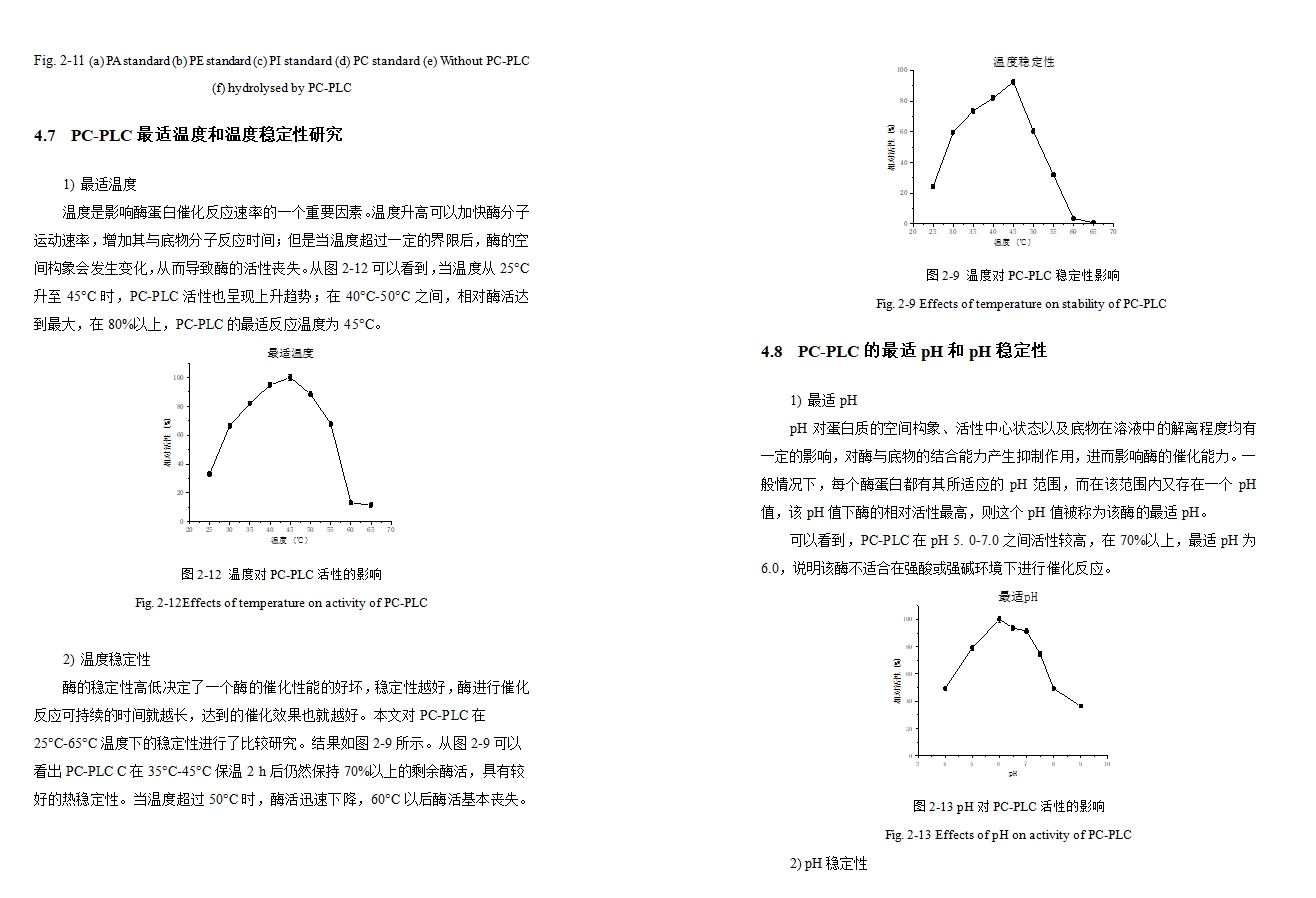
4.7 PC-PLC最适温度和温度稳定性研究 21
4.8 PC-PLC的最适PH和PH稳定性 23
4.9 金属离子对PC-PLC活性的影响 24
第五章 结论 25
参考文献 25
致谢 . 28
